Redox-Reaktionen I
Verbrennung von Magnesium – als Redox-Reaktion (2)
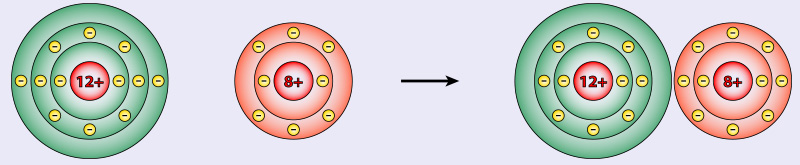
Aufgabe 4
Lies den Text und trage die unten stehenden Wörter richtig in die Lücken ein!
Anion Elektronenübertragung Kation Magnesium mehr negativ Oxidation positiv Reduktion Sauerstoff Valenzschale weniger




